メンバー
| リーダー |
研究部長 豊原 潤 |
|---|
| 研究員 |
坂田 宗之、多胡 哲郎 |
|---|
| 非常勤研究員 |
日浦 幹夫、山本 由美 |
|---|
キーワード
分子イメージング、PETトレーサー、初期臨床
主な研究
- 新規PETトレーサー開発
- 小動物イメージング研究
研究紹介
1.新規PETトレーサー開発
PET研究の発展は、その基礎となるPETトレーサーの開発に大きく依存しています。私たちは、加齢に伴う神経変性や認知症の診断、これらの病態機能の解明に役立つ新規PETトレーサーの開発を中心に研究活動を行っています。また、臨床研究に必要なPET薬剤の供給や画像解析ツールの開発も行って、PET画像診断研究テーマと連携して研究を進めています。当センターでは1990年の旧ポジトロン医学研究施設開設以来、これまでに54化合物のPETトレーサーの臨床利用を実現しており、そのうち10化合物は世界に先駆けて、当センターにおいて初めてヒトへ投与されました(図1)。
現在、脳内環境の維持に関連した新規PETトレーサーならびに神経変性疾患に関連があると考えられるヒストン脱アセチル化酵素に対する新規PETトレーサーの創薬研究を中心に展開しています。
新規PETトレーサー開発の一環として、PET薬剤製造法の開発、初期臨床研究における動態解析や被ばく線量評価、さらには被験者の検査負担を軽減する新しい診断法の開発も行っています。
PET薬剤科学研究はPET薬剤製造施設としてのPET薬剤製造部門・品質管理部門としての役割も果たしており、日本核医学会によるPET薬剤製造基準(学会GMP)認証や治験薬受託製造施設として、PET薬剤のGMP製造を行っています。
図1.当センターにて世界で初めてヒトへ投与されたPETトレーサー
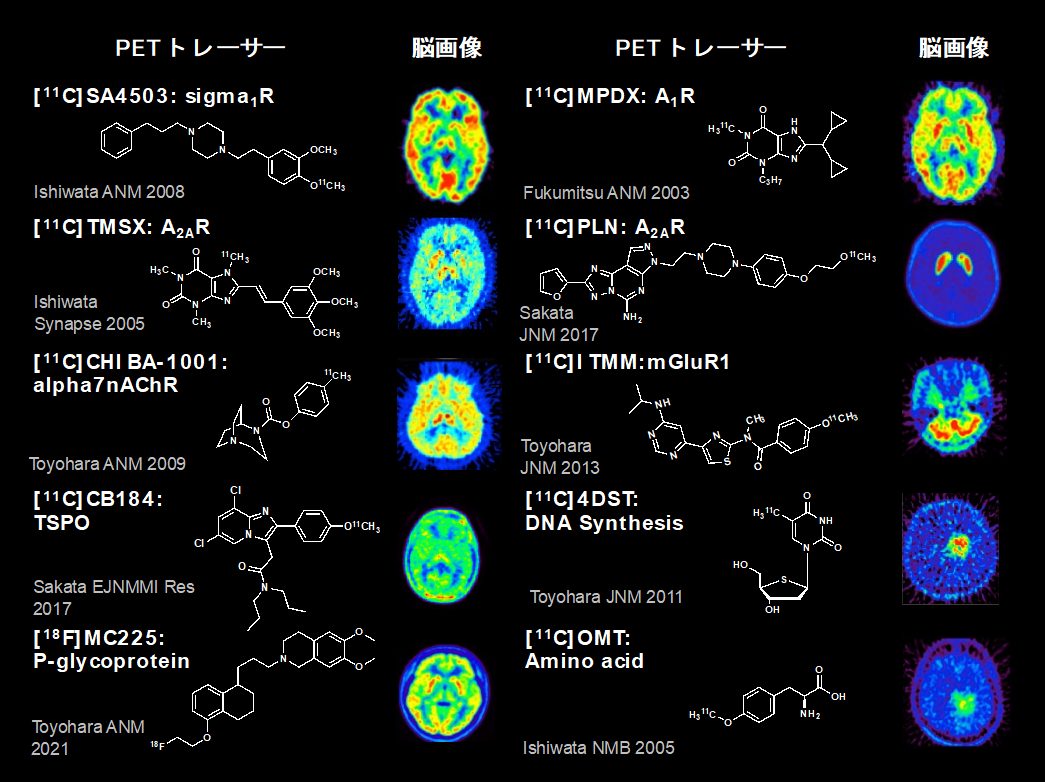
2.小動物イメージング研究
小動物専用のPETならびにMRIを用いて、マウス・ラットを対象とした、加齢に伴う生理機能の変化や疾患モデル動物における病態機能に関する研究を、所内の自然科学系研究テーマと連携して実施しています。2023年末にはPET装置が小動物専用の全身PET/CT装置(図2;Bruker社製Si-78)に更新され、同時に2013年に導入したMRI装置のソフトウエア更新も実施されました(図2;Bruker社製Icon)。これにより、マウス全身の動態計測が可能となりました。

図2.小動物専用全身PET/CT装置(Si-78)と小動物専用1T MRI装置(Icon)
参考資料
共同研究先へのリンク
共同研究先
主要文献
- Toyohara J., Komoda T., Tago T., Ito M., Yoshino H.: Light up heart-type fatty acid binding protein (FABP3) with a novel fluorine-18 labelled selective FABP3 ligand. EJNMMI. Res., 2024; 14(1):107.
- Toyohara J., Tago T., Sakata M.: Process validation and preclinical development of a new PET cerebral blood flow tracer [11C]MMP for initial clinical trials. EJNMMI. Radiopharm. Chem., 2024; 9(1):53.
- Tago T., Toyohara J.: Step-by-step optimization of the radiosynthesis of the brain HDAC6 radioligand [18F]FSW-100 for clinical applications. EJNMMI. Radiopharm. Chem., 2024; 9(1):45.
- Tago, T., Sakata, M., Kanazawa, M., Yamamoto, S., Ishii, K., Toyohara, J.: Preclinical validation of a novel brain-penetrant PET ligand for visualization of histone deacetylase 6: a potential imaging target for neurodegenerative diseases. Eur. J. Nucl. Med. Mol. Imaging., 2004; 51(8):2193-2203.
- Toyohara, J., Sakata, M., Wagatsuma, K., Tago, T., Ishibashi, K., Ishii, K., Eslinga, P., Ishiwata, K.: Test-retest reproducibility of cerebral adenosine A2A receptor quantification using [11C]preladenant. Ann. Nucl. Med., 2022; 36(1):15-23.
- Toyohara, J., Sakata, M., Ishibashi, K., Mossel, P., Imai, M., Wagatsuma, K., Tago, T., Imabayashi, E., Colabufo, N.A., Luurtsema, G., Ishii, K.: First clinical assessment of [18F]MC225, a novel fluorine-18 labelled PET tracer for measuring functional P-glycoprotein at the blood-brain barrier. Ann. Nucl. Med., 2021; 35(11):1240-1252.
- Tago, T., Toyohara, J., Ishii, K.: Preclinical evaluation of an 18F-labeled SW-100 derivative for PET imaging of histone deacetylase 6 in the brain. ACS. Chem. Neurosci., 2021; 12(4):746-755.
- Tago, T., Toyohara, J., Fujimaki, R., Tatsuta, M., Song, R., Hirano, K., Iwai, K., Tanaka, H.: Effects of 18F-fluorinated neopentyl glycol side-chain on the biological characteristics of stilbene amyloid-b PET ligands. Nucl. Med. Biol., 2021; 48(8):2615-2623.
- Toyohara, J., Nishino, K., Sakai, M., Tago, T., Oda, T.: Automated production of [18F]MK-6240 on CFN-MPS200. Appl. Radiat. Isot., 2021; 168:109468.
- Toyohara, J., Harada, N., Kakiuchi, T., Ohba, H., Kanazawa, M., Tago, T., Sakata, M., Ishiwata, K.: Synthesis and evaluation of N-isopropyl-p-[11C]methylamphetamine as a novel cerebral blood flow tracer for positron emission tomography. EJNMMI. Res., 2020; 10(1):115.
- Toyohara, J., Sakata, M., Tago, T., Colabufo, N.A., Luurtsema, G.: Automated synthesis, preclinical toxicity, and radiation dosimetry of [18F]MC225 for clinical use: a tracer for measuring P-glycoprotein function at the blood-brain barrier. EJNMMI. Res., 2020; 10(1):84.
- Tago, T., Toyohara, J., Ishii, K.: Radiosynthesis and preliminary evaluation of an 18F-labeled tubastatin A analog for PET imaging of histone deacetylase 6. J. Labelled. Comp. Radiopharm., 2020; 63(2):85-95.
- Toyohara, J., Yamamoto, H., Tago, T.: Searching for diagnostic properties of novel fluorine-18-labeled D-allose. Ann. Nucl. Med., 2019; 33(11):848-854.
- Tago, T., Toyohara, J., Sengoku, R., Murayama, S., Ishii, K.: Monoamine oxidase B binding of 18F-THK5351 to visualize glioblastoma and associated gliosis: an autopsy-confirmed case. Clin. Nucl. Med., 2019; 44(6):507-509.
- Tago, T., Toyohara, J., Harada, R., Furumoto, S., Okamura, N., Kudo, Y., Takahashi-Fujigasaki, J., Murayama, S., Ishii, K.: Characterization of the binding of tau imaging ligands to melanin-containing cells: putative off-target-binding site. Ann. Nucl. Med., 2019; 33(6): 375-382.
- Sakata, M., Toyohara, J., Ishibashi, K., Wagatsuma, K., Ishii, K., Zhang, M.R., Ishiwata, K.: Age and gender effects of 11C-ITMM binding to metabotropic glutamate receptor type 1 in healthy human participants. Neurobiol. Aging., 2017; 55:72-77.
- Sakata, M., Ishibashi, K., Imai, M., Wagatsuma, K., Ishii, K., Hatano, K., Ishiwata, K., Toyohara, J.: Assessment of safety, efficacy, and dosimetry of a novel 18-kDa translocator protein ligand, [11C]ITMM, in healthy human volunteers. EJNMMI. Res., 2017; 7(1):26.
- Sakata, M., Ishibashi, K., Imai, M., Wagatsuma, K, Ishii, K., Zhou, X., de Vries, E.F.J., Elsinga, P.H., Ishiwata, K., Toyohara, J.: Initial evaluation of an adenosine A2A receptor ligand, 11C-preladenat, in healthy human subjects. J. Nucl. Med., 2017; 58(9):1464-1470.
- Toyohara, J., Sakata, M., Hatano, K., Yanai, S., Endo, S., Ishibashi, K., Wagatsuma, K., Ishii, K., Ishiwata, K.: Preclinical and first-in-human studies of [11C]CB184 for imaging the 18-kDa translocator protein by positron emission tomography. Ann. Nucl. Med., 2016; 30(8):53334-543.
- Toyohara, J., Okamoto, M., Aramaki, H., Zaitsu, Y., Shimizu, I., Ishiwata, K.: (R)-[11C]Emopamil as a novel tracer for imaging enhanced P-glycoprotein function. Nucl. Med. Biol., 2016; 43(1):52-62.
- Toyohara, J., Sakata, M., Oda, K., Ishii, K., Ito, K., Hiura, M., Fujinaga, M., Yamasaki, T., Zhang, M.R., Ishiwata, K.: Initial human PET studies of metabotropic glutamate receptor type 1 ligand 11C-ITMM. J. Nucl. Med., 2013; 54(8):1302-1307.
- Sakata, M., Oda, K., Toyohara, J., Ishii, K., Nariai, T., Ishiwata, K.: Direct comparison of radiation dosimetry of six PET tracers using human whole-body imaging and murine biodistribution studies. Ann. Nucl. Med., 2013; 27(3):285-296.
- Toyohara, J., Sakata, M., Fujinaga, M., Yamasaki, T., Oda, K, Ishii, K., Zhang, M.R., Moriguchi Jeckel, C.M., Ishiwata, K.: Preclinical and the first clinical studies on [11C]ITMM for mapping metabotropic glutamate receptor subtype 1 by positron emission tomography. Nucl. Med. Biol., 2013; 40(20:240-244.
- Toyohara, J., Sakata, M., Oda, K., Ishii, K., Ishiwata, K.: Longitudinal observation of [11C]4DST uptake in turpentine-induced inflammatory tissue. Nucl. Med. Biol., 2013; 40(20):240-244.
- Toyohara, J., Kobayashi, T., Mita, S., Ishiwata, K.: Application of [11C]SA4503 to selection of novel s1 selective agonists. Nucl. Med. Biol., 2012; 39(8):1117-1121.
- Toyohara, J., Sakata, M., Ishiwata, K.: Re-evaluation of in vivo selectivity of [11C]SA4503 to s1 receptors in the brain: contributions of emopamil binding protein. Nucl. Med. Biol., 2012; 39(7):1049-1052.
- Toyohara, J., Elsinga, P.H., Ishiwata, K., Sijbesma, J.W., Dierckx, R.A., van Waarde, A.: Evaluation of 4'-[methyl-11C]thiothymidine in a rodent tumor and inflammation model. J. Nucl. Med., 2012; 53(3):488-494.
- Toyohara, J., Nariai, T., Sakata, M., Oda, K., Ishii, K., Kawabe, T., Irie, T., Saga, T., Kubota, K., Ishiwata, K.: Whole-body distribution and brain tumor imaging with 11C-4DST: a pilot study. J. Nucl. Med., 2011; 52(8):1322-1328.
- Toyohara, J., Ishiwata, K., Sakata, M., Wu, J., Nishiyama, S., Tsukada, H., Hashimoto, K.: In vivo evaluation of carbon-11-labelled non-sarcosine-based glycine transporter 1 inhibitors in mice and conscious monkeys. Nucl. Med. Biol., 2011; 38(4):517-527.
- Sakata, M., Wu, J., Toyohara, J., Oda, K., Ishikawa, M., Ishii, K., Hashimoto, K., Ishiwata, K.: Biodistribution and radiation dosimetry of the a7 nicotinic acetylcholine receptor ligand [11C]CHIBA-1001 in humans. Nucl. Med. Biol., 2011; 38(3):443-448.
- Toyohara, J., Ishiwata, K., Sakata, M., Wu, J., Nishiyama, S., Tsukada, H., Hashimoto, K.: In vivo evaluation of alpha7 nicotinic acetylcholine receptor agonists [11C]A-582941 and [11C]A-844606 in mice and conscious monkeys. PLos. One., 2010; 5(2):e8961.
- Toyohara, J., Sakata, M., Wu, J., Ishikawa, M., Oda, K., Ishii, K., Iyo, M., Hashimoto, K., Ishiwata, K.: Preclinical and the first clinical studies on [11C]CHIBA-1001 for mapping alpha7 nicotinic receptors by positron emission tomography. Ann. Nucl. Med., 2009; 23(3):301-309.
